*31% mindre forverring av kognitive symptomer og funksjoner over 18 måneder hos lecanemab-behandlede pasienter sammenlignet med placebogruppen (gjennomsnittlig endring fra baseline ifølge CDR-SB var 1,22 sammenlignet med 1,75; forskjell mellom grupper −0,535; 95% KI −0,778; −0,293).1
Administrering av LEQEMBI® og informasjon ved behandling1

LEQEMBI skal fortynnes før intravenøs infusjon.
Under behandling med LEQEMBI bør testing av kognitiv funksjon og klinisk vurdering av symptomer skje omtrent hver 6. måned. De kognitive testene og utviklingen av symptomer bør brukes for å vurdere om pasienten har progrediert til moderat Alzheimers sykdom og/eller om det kliniske forløpet ellers antyder at LEQEMBI ikke har vist effekt hos pasienten, og gi grunnlag for en beslutning om behandlingen med LEQEMBI skal avsluttes.
Behandlingen med LEQEMBI skal avsluttes når pasienten progredierer til moderat Alzheimers sykdom.1
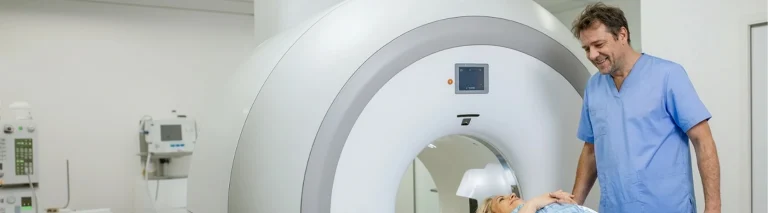
Behandlingen skal initieres og overvåkes av leger med erfaring i diagnostikk og behandling av Alzheimers sykdom og med rask tilgang til magnetresonanstomografi (MR). Infusjoner av LEQEMBI skal administreres av kvalifisert helsepersonell som er utdannet til å overvåke, gjenkjenne og håndtere infusjonsrelaterte reaksjoner.
Ett 5 ml hetteglass inneholder 500 mg LEQEMBI (500mg/5ml)
Parenterale legemidler skal kontrolleres visuelt med hensyn til partikler og misfarging før administrering. Hvis noe av dette observeres, skal legemidlet kasseres.
Beredning av infusjonsløsning1
Beregn dosen, den totale volumet av løsningen med LEQEMBI som kreves og antallet injeksjonsflasker som trengs basert på pasientens faktiske kroppsvekt. Hver injeksjonsflaske inneholder en konsentrasjon av LEQEMBI på 100 mg/ml. .
Trekk ut nødvendig dose LEQEMBI fra injeksjonsflasken/flaskene og tilsett til 250 ml 9 mg/ml (0,9%) natriumkloridløsning for injeksjon.
Vend forsiktig infusjonsposen som inneholder den fortynnede løsningen med LEQEMBI slik at den blandes helt. Ikke rist posen.
Infusjonsposer laget av polypropen, polyvinylklorid, samekstrudert polyolefin/polyamid eller eten/propen-sampolymer har blitt bekreftet å være kompatible for administrering av LEQEMBI.
Etter fortynning anbefales umiddelbar bruk.
Holdbarhet1
Kjemisk og fysisk stabilitet ved bruk har blitt påvist i 24 timer ved 25°C. Fra et mikrobiologisk synspunkt bør produktet brukes umiddelbart, med mindre fortynningsmetoden utelukker risikoen for mikrobiell kontaminering. Hvis produktet ikke brukes umiddelbart, er det brukeren som er ansvarlig for oppbevaringstider og oppbevaringsforhold før bruk.
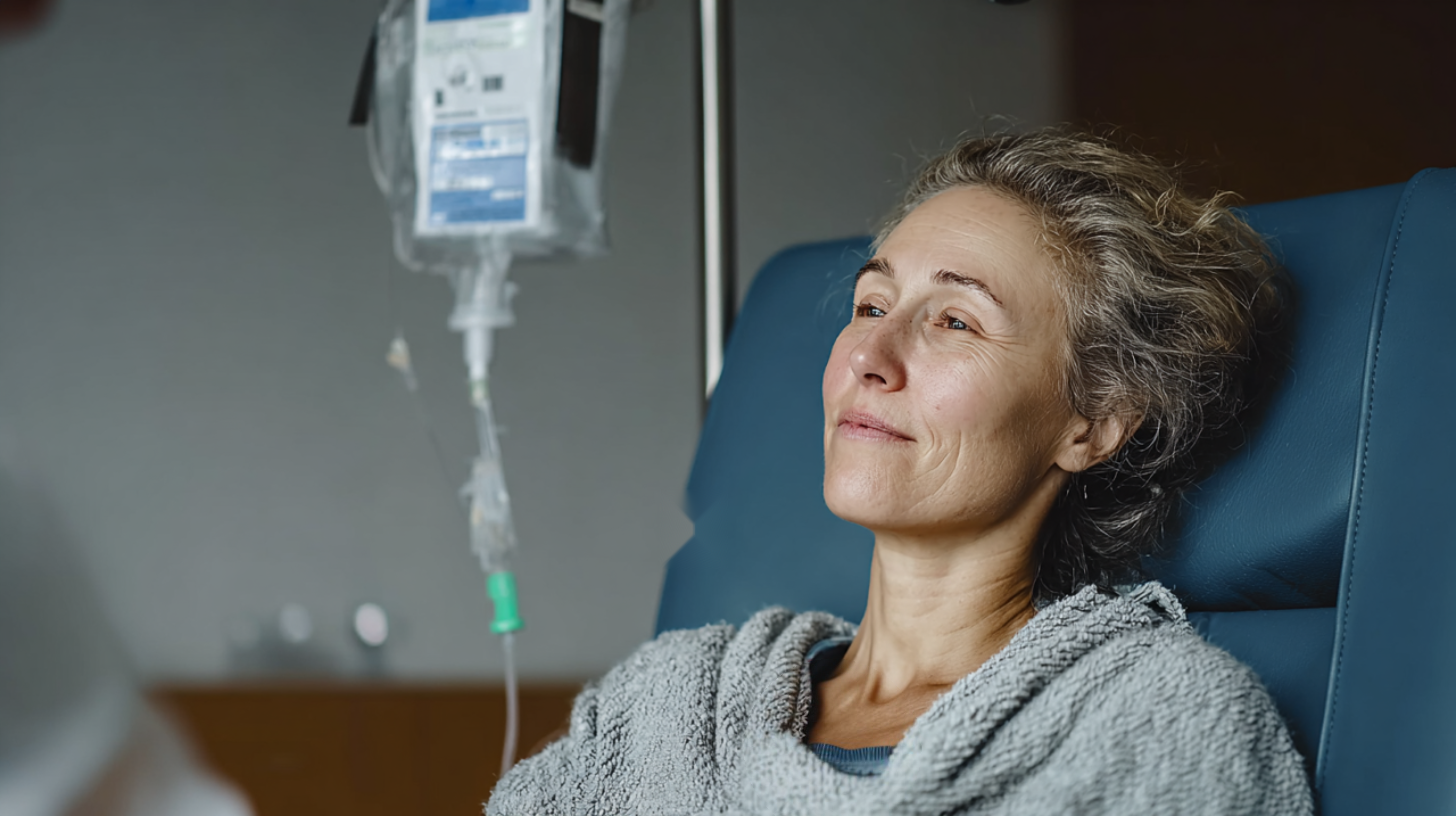
Administrering av infusjonsløsning1
La den fortynnede løsningen med LEQEMBI varme opp til romtemperatur før infusjonen.
Administrer hele dosen av LEQEMBI intravenøst over cirka 1 time gjennom en intravenøs slange som inneholder et terminalt lavproteinbindende inline-filter på 0,2 mikrometer (kompatible filtermaterialer inkluderer polytetrafluoreten, polyetersulfon, polykarbonat, polyvinylidenfluorid, polypropen, polyuretan og polysulfon). Skyll infusjonsslangen for å sikre at alt LEQEMBI administreres.
Ubrukt legemiddel og avfall skal kasseres i henhold til gjeldende anvisninger.
Referanser
1. LEQEMBI Preparatomtale Avsnitt 4.2, 6.3, 6.6