Hva er en klinisk relevant effekt ved en sykdomsmodifiserende behandling?
Hva er en klinisk relevant effekt ved en sykdomsmodifiserende behandling?
Betydningsfull gevinst ved behandling av Alzheimers sykdom
For å evaluere meningsfull nytte av behandlingen av Alzheimers sykdom (AD), er det avgjørende å ta hensyn til de ulike stadiene av sykdommen. Det er ikke nok å bare sammenligne statistiske p-verdier mellom behandlings- og placebogruppene i kliniske studier. I stedet må man evaluere hvilke tiltak som ble brukt og omfanget av forskjellen mellom gruppene over tid for å få et klarere bilde av nytten av behandlingen.1
Sykdomsstadier ved Alzheimers sykdom og valg av utfallsmål
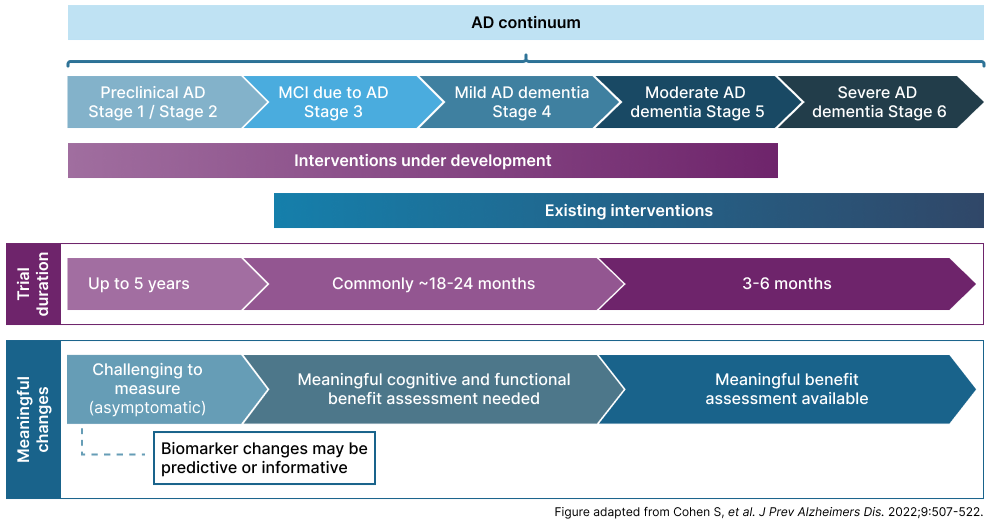
Alzheimers sykdom rammer ulike områder av hjernen, hvor symptombildet varierer avhengig av hvilket stadium av sykdommen pasienten er i. National Institute of Aging-Alzheimer’s Association (NIA-AA) klassifiserer disse stadiene fra 0–6, som gjenspeiler sykdommens kliniske forløp; fra preklinisk Alzheimers sykdom med biomarkører uten symptomer, til MCI (mild kognitiv svikt) og til slutt demens (mild, moderat og alvorlig), (se figur).1,2
I de tidlige stadiene av sykdommen kan meningsfull nytte kun måles med biomarkører fordi det ennå ikke er noen symptomer på sykdommen, mens funksjonelle og kognitive utfall er relevante i de senere stadiene. Det er derfor viktig å velge utfallsmål som er relevante for det spesifikke sykdomsstadiet når man vurderer nytten av behandlingen.1
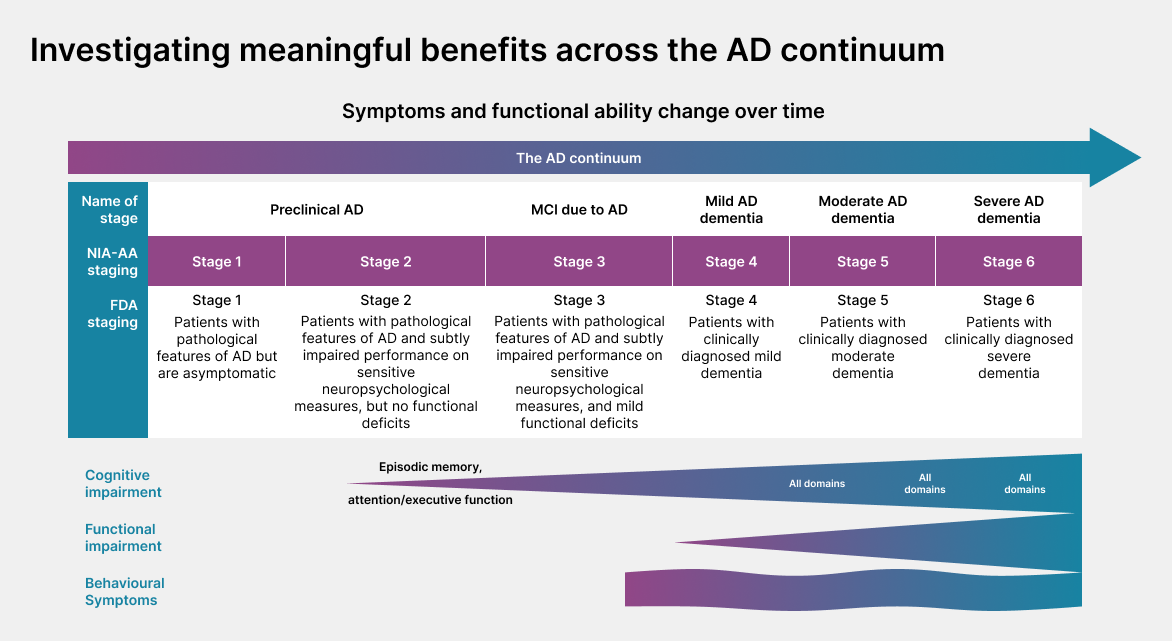
AD, Alzheimer’s disease; ADL, activities of daily living; FDA, Food and Drug Administration; MCI, mild cognitive impairment; MMSE, Mini-Mental State Examination; NIA-AA, National Institute of Aging–Alzheimer’s Association. Figure adapted from Cohen S, et al. J Prev Alzheimers Dis. 2022;9:507–522.
Tester for å måle kognitive og funksjonelle utfall
Vanlige tester som brukes til å måle kognitive utfall er ADAS-Cog og MMSE, mens ADCS-ADL, A-IADL-Q og FAQ brukes til å evaluere funksjon i hverdagen.1,5-7 CDR-SB (Clinical Dementia Rating-Sum of Boxes) er en 18-punkts vurderingsskala som brukes til å måle både kognitiv evne og funksjon (se tabell).8,9 Denne skalaen brukes ofte i anti-amyloidstudier, spesielt hos symptomatiske pasienter.1
ADAS-Cog = Alzheimer’s Disease Assessment Scale – Cognitive Subscale
MMSE = Mini Mental State Examination
ADCS-ADL = Alzheimer’s Disease Cooperative Study – Activities of Daily Living
A-IADL-Q= Amsterdam Instrumental Activities of Daily Living Questionnaire
FAQ =Functional Activities Questionnaire
Clinical Dementia Rating (CDR)
| 0 | 0.5 | 1 | 2 | 3 |
|---|
| CDR sum of boxes range2 | 0.5-2.5 | 3.0-4.0 | 4.5-9.0 | 9.5-15.5 | 16.0-18.0 |
|---|---|---|---|---|---|
| Staging category2 | Questionable impairment | Very mild dementia | Mild dementia | Moderate dementia | Severe dementia |
| Score only as decline from previous usual level due to cognitive loss, not impairment due to other factors | |||||
| I M P A I R M E N T1 | |||||
|---|---|---|---|---|---|
| None (0) | Questionable (0.5) | Mild (1) | Moderate (2) | Severe (3) | |
| Memory | No memory loss or slight inconsistent forgetfulness | Consistent slight forgetfulness; partial recollection of events; “benign” forgetfulness | Moderate memory loss; more marked for recent events; defect interferes with everyday activities | Severe memory loss; only highly learned material retained; new material rapidly lost | Severe memory loss; only fragments remain |
| Orientation | Fully oriented | Fully oriented except for slight difficulty with time relationships | Moderate difficulty with time relationships; oriented for place at examination; may have geographical disorientation elsewhere | Severe difficulty with time relationships; usually disoriented to time, often to place | Oriented to person only |
| Judgment & problem solving | Solves everyday problems & handles business & financial affairs well; judgment good in relation to past performance | Slight impairment in solving problems, similarities, and differences | Moderate difficulty in handling problems, similarities, and differences; social judgment usually maintained | Severely impaired in handling problems, similarities, and differences; social judgment usually impaired | Unable to make judgments or solve problems |
| Community affairs | Independent function at usual level in job, shopping, volunteer & social groups | Slight impairment in these activities | Unable to function independently at these activities although may still be engaged in some; appears normal to casual inspection | No pretence of independent function outside home | |
| Appears well enough to be taken to functions outside a family home | Appears too ill to be taken to functions outside a family home | ||||
| Home and hobbies | Life at home, hobbies, and intellectual interests well maintained | Life at home, hobbies, and intellectual interests slightly impaired | Mild but definite impairment of function at home; more difficult chores abandoned; more complicated hobbies and interests abandoned | Only simple chores preserved; very restricted interests, poorly maintained | No significant function in home |
| Personal care | Fully capable of self-care | Needs prompting | Requires assistance in dressing, hygiene, keeping of personal effects | Requires much help with personal care; frequent incontinence | |
1. Morris JS, Neurology 1993; 43:2412-2414; 2. O´Bryant, et al. Arch Neurol. 2008;65:1091-1096
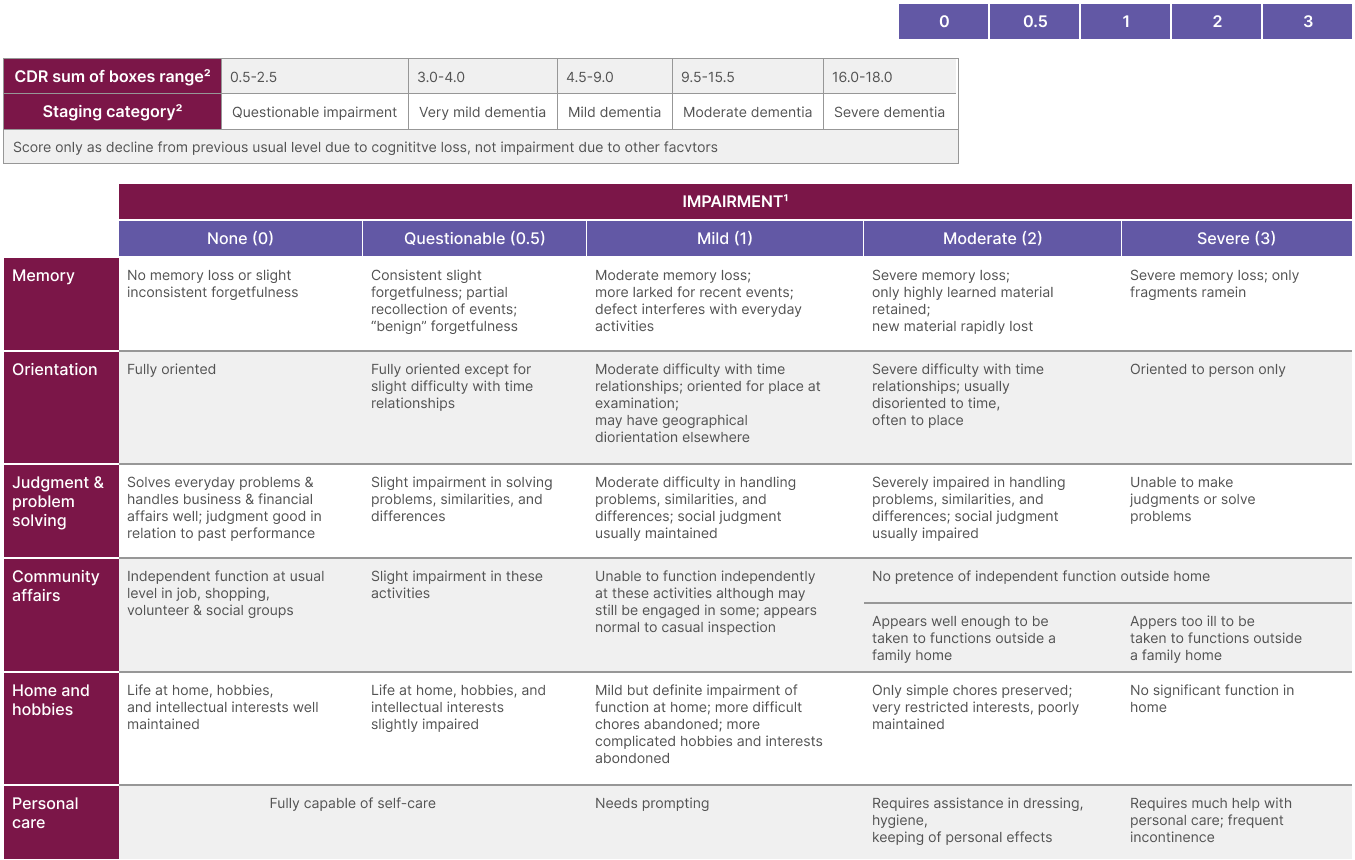
En forskjell på 0,5 på CDR-SB-skalaen kan bety at en pasient som tidligere ikke hadde noen symptomer, eller bare svært subtile, nå opplever betydelige symptomer som påvirker dagliglivet. Dette kan innebære at man må skrive notater for å huske oppgaver, eller at man går fra å være selvstendig til å trenge hjelp.8
Skalaen ble opprinnelig utviklet for å evaluere personer i demensstadiet og blir mer sensitiv etter hvert som sykdommen utvikler seg fra MCI til demens, hvor skårene akkumuleres og øker raskt. Ved preklinisk AD (stadium 2) vurderes ingen skår på skalaen, mens pasienter i MCI-fasen (stadium 3) kan vurderes til en skår mellom 0,5 og 2,5. Rapportering av forskjeller på CDR-SB-skalaen på ett bestemt tidspunkt er ofte mindre meningsfullt ved sykdomsmodifiserende behandlinger, ettersom nytten forventes å øke over tid.8,21
Forskjellen mellom symptomlindrende og sykdomsmodifiserende behandling
Symptomatisk behandling gir en midlertidig nytte som kan forbedre ADL eller kognitiv funksjon så lenge legemiddelet tas, men behandlingen bremser ikke sykdomsprogresjonen. Effekten kan også avta over tid, spesielt ved alvorlig demens. Dette beror på at sykdommen fortsetter å utvikle seg og påvirke hjernen, noe som gjør denne typen behandling mindre effektiv i å lindre symptomer etter hvert som sykdommen utvikler seg.
Sykdomsmodifiserende behandling, derimot, retter seg mot den underliggende årsaken til sykdommen og bremser sykdomsprogresjonen på lang sikt, med effekt på kognisjon og funksjon. Derfor er det viktig å starte behandlingen tidlig og gi behandling kontinuerlig. Ved sykdomsmodifiserende behandling bør effekten gradvis øke over tid. Dette beskrives best med begreper som «vedvarende sykdomsforsinkelse» fordi det beskriver effekten på tvers av hele sykdomsforløpet, ikke bare en liten del.10-12
Fra et klinisk perspektiv reduserer anti-amyloidbehandling mengden amyloid-β-plakk i hjernen og har også en innvirkning på nedstrøms mekanismer, som endringer i tau, som er nært knyttet til kliniske symptomer og sykdomsprogresjon13,14
Kliniske studier og smalt tidsvindu
Kliniske studier gir et begrenset bilde av sykdomsprogresjon fordi de ofte bare dekker en liten del av sykdomsforløpet. Prekliniske studier gjenspeiler bare noen få år av hele den prekliniske fasen, som vanligvis er lengre enn et tiår, noen ganger kanskje til og med to tiår. Dette gjelder også for pågående kliniske studier som reflekterer senere stadier av sykdommen (se figur).1,15,16
Trial design and disease stage
AD, Alzheimer’s disease; MCI, mild cognitive impairment. 1. Cohen S,et al. J Prev Alzheimers Dis.2022;9:507-522; 2. Porsteinsson AP, et al. J Prev Alzheimers Dis. 2021;3:371-386;3. Cummings J, et al. Alz res Therapy. 2019;11:76.
Definisjon av betydningsfull gevinst av sykdomsmodifiserende behandling
langsommere sykdomsprogresjon
økning i forskjellen mellom behandlings- og placebogruppene
økt tid til hendelse (spart tid til progresjon)
endringer i biomarkører som forutsier fremtidig klinisk nytte
resultatene bør oppnås med en gunstig risiko-nytte-profil
Mens farmakologiske effekter av symptomatisk behandling kan observeres i løpet av timer eller dager, forventes effekten av sykdomsmodifiserende behandlinger å øke over tid.
Fordi de sykdomsmodifiserende effektene kanskje ikke fremstår tydelig under korte kliniske studier, kan langsiktige (legemiddel-placebo-forskjeller) vurderes ved hjelp av statistiske modeller av sykdomsprogresjon og behandlingsrespons.
Et viktig aspekt ved sykdomsmodifiserende behandlinger er evnen til å forsinke progresjonen til et visst stadium av sykdommen. For pasienten er det relevant å snakke om å vinne tid frem til demensstadiet, som mange frykter mest. Den ekstra tiden pasienten kan klare daglige aktiviteter uten omfattende hjemmesykepleie eller utsettelse av overføring til sykehjem.3
Referanser
1. Cohen S, et al. Clinical Trial Endpoints and Their Clinical Meaningfulness in Early Stages of Alzheimer’s Disease. J Prev Alzheimers Dis. 2022;9(3):507–22.
2. Petersen RC, et al. Expectations and clinical meaningfulness of randomized controlled trials. Alzheimers Dement. 2023;19(6):2730–6.
3. Cummings J, et al. Defining Disease Modifying Therapy for Alzheimer’s Disease. J Prev Alzheimers Dis. 2017;4(2):109–15.
4. Tochel C, et al. What outcomes are important to patients with mild cognitive impairment or Alzheimer’s disease, their caregivers, and health-care professionals? A systematic review. Alzheimers Dement Diagn Assess Dis Monit. 2019;11(1):231–47.
5. Kueper JK, et al. The Alzheimer’s Disease Assessment Scale-Cognitive Subscale (ADAS-Cog): modifications and responsiveness in pre-dementia populations. J Alzheimers Dis. 2018;63(2):423–44.
6. Galasko D, et al. An inventory to assess activities of daily living for clinical trials in Alzheimer’s disease. Alzheimer Dis Assoc Disord. 1997;11(Suppl 2):S33–9.
7. Nosheny RL, et al. The Evaluation of the Electronic Clinical Dementia Rating for Dementia Screening. JAMA Netw Open. 2023;6(9):e2333786.
8. Morris JC. The Clinical Dementia Rating (CDR): current version and scoring rules. Neurology. 1993;43(11):2412–4.
9. O’Bryant SE, et al. Staging dementia using Clinical Dementia Rating Scale sum of boxes scores: a Texas Alzheimer’s Research Consortium study. Arch Neurol. 2008;65(8):1091–5.
10. Cummings J, et al. Defining disease modifying therapy for Alzheimer’s disease. J Prev Alzheimers Dis. 2017;4(2):109–15.
11. Atri A. Current and Future Treatments in Alzheimer’s Disease. Semin Neurol. 2019;39(2):227–40.
12. Assunção SS, et al. Meaningful benefits: a framework to assess disease-modifying therapies in preclinical and early Alzheimer’s disease. Alzheimers Res Ther. 2022;14(1):54.
13. Jack CR Jr, et al. NIA-AA research framework: toward a biological definition of Alzheimer’s disease. Alzheimers Dement. 2018;14(4):535–62.
14. Jack CR Jr, et al. Revised criteria for the diagnosis and staging of Alzheimer’s disease. Nat Med. 2024 Jun 27. Epub ahead of print.
15. Porsteinsson AP, et al. Diagnosis of early Alzheimer’s disease: clinical practice in 2021. J Prev Alzheimers Dis. 2021;8(3):371–86.
16. Cummings J, et al. The “rights” of precision drug development for Alzheimer’s disease. Alzheimers Res Ther. 2019;11:76.
17. Eisai Co., Ltd. LEQEMBI (lecanemab) product information [Internett]. [sitert 2025 aug 27]. Tilgjengelig fra: https://www.ema.europa.eu/en/medicines/human/EPAR/leqembi
18. Klunk WE, et al. Imaging brain amyloid in Alzheimer’s disease with Pittsburgh Compound-B. Ann Neurol. 2004;55(3):306–19.
19. Mohs RC, et al. Development of cognitive instruments for use in clinical trials of antidementia drugs: additions to the Alzheimer’s Disease Assessment Scale that broaden its scope. Alzheimer Dis Assoc Disord. 1997;11(Suppl 2):S13–21.
20. Wang J, et al. ADCOMS: a composite clinical outcome for prodromal Alzheimer’s disease trials. J Neurol Neurosurg Psychiatry. 2016;87(9):993–9.
21. Cummings J, et al. Meaningful benefit and minimal clinically important difference (MCID) in Alzheimer’s disease: open peer commentary. Alzheimers Dement (N Y). 2023;9:e12411.