

*31% mindre forverring av kognitive symptomer og funksjoner over 18 måneder hos lecanemab-behandlede pasienter sammenlignet med placebogruppen (gjennomsnittlig endring fra baseline ifølge CDR-SB var 1,22 sammenlignet med 1,75; forskjell mellom grupper −0,535; 95% KI −0,778; −0,293).1
LA pasientene bli lenger i et tidligere stadium av sykdommen med tidlig og kontinuerlig behandling med LEQEMBI®
Mer tid i et mildere sykdomsstadium 1
- Pasienter som fikk LEQEMBI ble værende i et mildere sykdomsstadium lenger*, målt med CDR-SB (kognitiv og funksjonell vurderingsskala) sammenlignet med placebo.
Effekten øker med tiden1
- Effekten av LEQEMBI-behandling øker over 18 måneder.
Resultatene er statistisk signifikante på alle primære endepunkter1
- LEQEMBI–behandlingen førte til konsekvent langsommere sykdomsprogresjon, også vist med ADAS-Cog14 og ADCS-MCI-ADL, samt en reduksjon av amyloid-β (amyloid-PET), hver med statistisk signifikans sammenlignet med placebo.

*31% mindre forverring av kognitive symptomer og funksjoner over 18 måneder hos lecanemab-behandlede pasienter sammenlignet med placebogruppen (gjennomsnittlig endring fra baseline ifølge CDR-SB var 1,22 sammenlignet med 1,75; forskjell mellom grupper −0,535; 95% KI −0,778; −0,293).1
LEQEMBI – Langsommere progresjon betyr mer selvstendig tid1
CDR-SB: 31% bremsing i forverringen* av kognitive symptomer og funksjoner1
Målt over 18 måneder sammenlignet med placebo hos pasienter med Alzheimers sykdom (AD), målt med Clinical Dementia Rating Scale (CDR-SB).
*Justert gjennomsnittlig endring fra baseline på CDR-SB 1,217 sammenlignet med 1,752; gruppeskille −0,535; 95% KI (−0,778, −0,293).
- hukommelse
- orienteringsevne
- dømmekraft
- problemløsningsferdigheter
- sosiale/allmenne aktiviteter
- hjem og fritid
- personlig hygiene
ADCS MCI-ADL: 33% mindre forverring° i evnen til å utføre daglige oppgaver (ADL)1
Målt over 18 måneder, sammenlignet med placebo hos pasienter med AD, målt med ADC MCI-ADL..
°Justert gjennomsnittlig endring fra baseline på ADAS MCI-ADL −3,873 sammenlignet med −5,809; gruppeskille 1,936; 95% KI (1,029; 2,844).
- betale regninger
- navigere utenfor hjemmet, gå og handle
- bruke husholdningsapparater
- finne personlige eiendeler
- kle på seg
- klare seg alene hjemme
ADAS-Cog14: 26% mindre forverring§ i kognitiv evne1
Målt over 18 måneder, sammenlignet med placebo hos pasienter med AD, målt med ADAS-Cog14.
§Justert gjennomsnittlig endring fra baseline på ADAS Cog14 4,389 sammenlignet med 5,901; gruppeskille −1,512; 95% KI (−2,486; −0,538).
ADAS-Cog:
- ordgjenkjenning
- forsinket ordhukommelse
- ordhukommelse
- orientering
ADCS-iADL:
- lage mat
- telefonsamtaler
- handle
- komme i tide til helseavtaler og lignende
- være alene hjemme m.m.
LEQEMBI® – LÅNGSAMMARE PROGRESSION BETYDER MER OBEROENDE TID
LEQEMBI® 10 mg/kg varannan vecka N= 757, jämfört med placebo n= 764, indicerad population.
CDR-SB: 31% bremsing i forverringen* av kognitive symptomer og funksjoner1
*Justert gjennomsnittlig endring fra baseline på CDR-SB 1,217 sammenlignet med 1,752; gruppeskille −0,535; 95% KI (−0,778, −0,293).
- hukommelse
- orienteringsevne
- dømmekraft
- problemløsningsferdigheter
- sosiale/allmenne aktiviteter
- hjem og fritid
- personlig hygiene
Målt over 18 måneder sammenlignet med placebo hos pasienter med Alzheimers sykdom (AD), målt med Clinical Dementia Rating Scale (CDR-SB).
ADCS MCI-ADL: 33% mindre forverring° i evnen til å utføre daglige oppgaver (ADL)1
°Justert gjennomsnittlig endring fra baseline på ADAS MCI-ADL −3,873 sammenlignet med −5,809; gruppeskille 1,936; 95% KI (1,029; 2,844).
- betale regninger
- navigere utenfor hjemmet, gå og handle
- bruke husholdningsapparater
- finne personlige eiendeler
- kle på seg
- klare seg alene hjemme
Målt over 18 måneder, sammenlignet med placebo hos pasienter med AD, målt med ADC MCI-ADL..
ADAS-Cog14: 26% mindre forverring§ i kognitiv evne1
§Justert gjennomsnittlig endring fra baseline på ADAS Cog14 4,389 sammenlignet med 5,901; gruppeskille −1,512; 95% KI (−2,486; −0,538).
ADAS-Cog:
- ordgjenkjenning
- forsinket ordhukommelse
- ordhukommelse
- orientering
ADCS-iADL:
- lage mat
- telefonsamtaler
- handle
- komme i tide til helseavtaler og lignende
- være alene hjemme m.m.
Målt over 18 måneder, sammenlignet med placebo hos pasienter med AD, målt med ADAS-Cog14.
RESULTAT FOR CDR-SB, ADAS-COG14 OG ADCS MCI-ADL I CLARITY-AD1
| Indikert populasjon | ||
|---|---|---|
| Klinisk effektmål | LEQEMBI 10 mg/kg hver annen uke | Placebo |
| CDR-SB | N=757 | N=764 |
| Gjennomsnitt ved baseline (SD) | 3.18 (1.346) | 3.23 (1.343) |
| Justert gjennomsnittlig forandring fra baseline ved 18 måneder sammenlignet med placebo (95% KI) | 1.217 -0.535 (-0.778, -0.293) | 1.752 |
| ADAS-Cog14 | N=757 | N=764 |
| Gjennomsnitt ved baseline (SD) | 24.46 (7.081) | 24.40 (7.576) |
| Justert gjennomsnittlig forandring fra baseline ved 18 måneder sammenlignet med placebo (95% KI) | 4.389 -1.512 (-2.486, -0.538) | 5.901 |
| ADCS MCI-ADL | N=757 | N=764 |
| Gjennomsnitt ved baseline (SD) | 41.15 (6.616) | 40.72 (6.937) |
| Justert gjennomsnittlig forandring fra baseline ved 18 måneder sammenlignet med placebo (95% KI) | -3.873 1.936 (1.029, 2.844) | -5.809 |
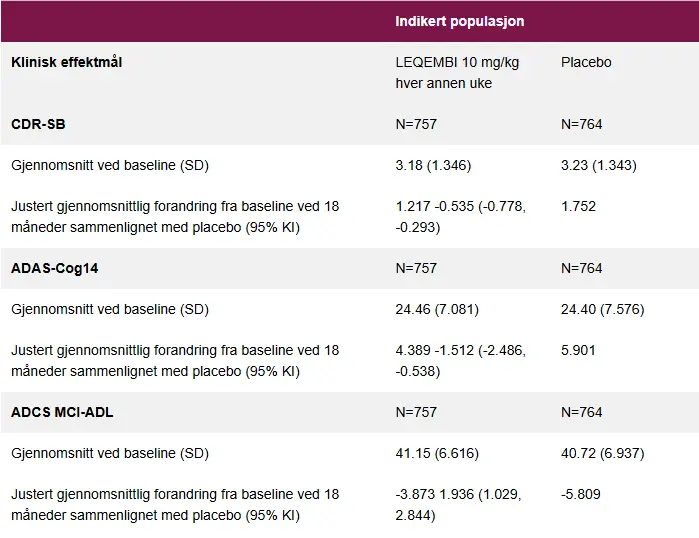
CDR-SB = Clinical Dementia Rating – sum of boxes. ADAS-Cog14 = Alzheimer’s Disease Assessment Scale.° ADAS MCI-ADL = Alzheimer’s Disease Cooperative Study-Activities of Daily Living Scale for Mild Cognitive Impairment.
Effekten av LEQEMBI ble klinisk evaluert i en dobbeltblindet, placebokontrollert, randomisert studie som omfattet pasienter med tidlig Alzheimers sykdom og bekreftet amyloidpatologi:
Det primære effektmålet var endring fra baseline ved 18 måneder i CDR-SB.
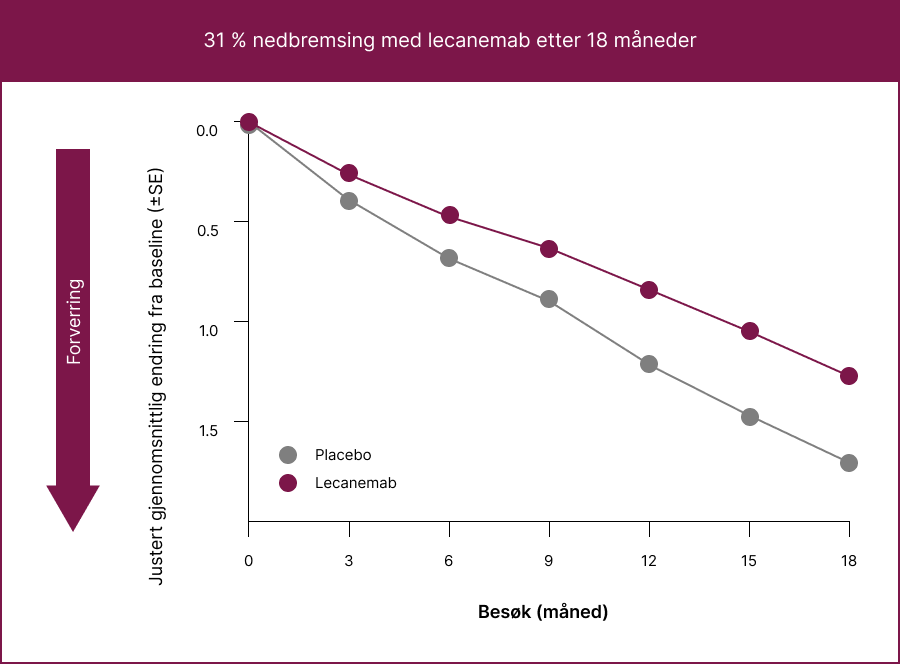
Over 18 måneder, bremset LEQEMBI forverringen av kognitive symptomer og funksjoner med 31% sammenlignet med placebo, målt med CDR-SB i den indikerte populasjonen.
ADCS MCI-ADL: 33 % mindre forverring° i pasientenes evne til å utføre daglige aktiviteter (ADL)
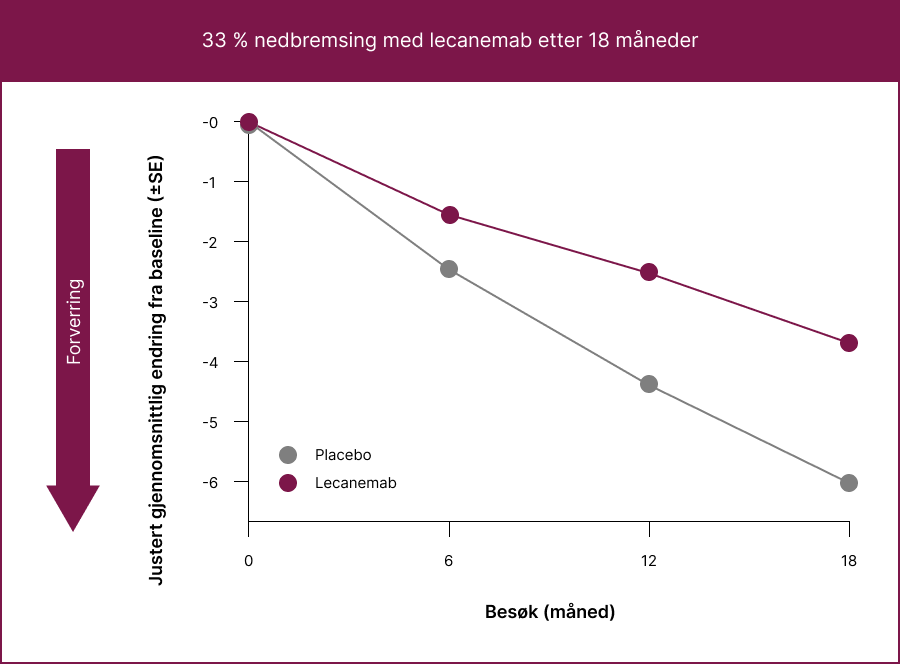
LEQEMBI bremset sykdomsprogresjonen betydelig i henhold til ADCS MCI-ADL-skalaen med 33 % etter 18 måneder og på alle tidspunkter fra 6 måneder.1
° ADAS MCI-ADL = Alzheimer’s Disease Cooperative Study-Activities of Daily Living Scale for Mild Cognitive Impairment.
ADAS-Cog 14: 26 % mindre forverring§ av kognitiv evne
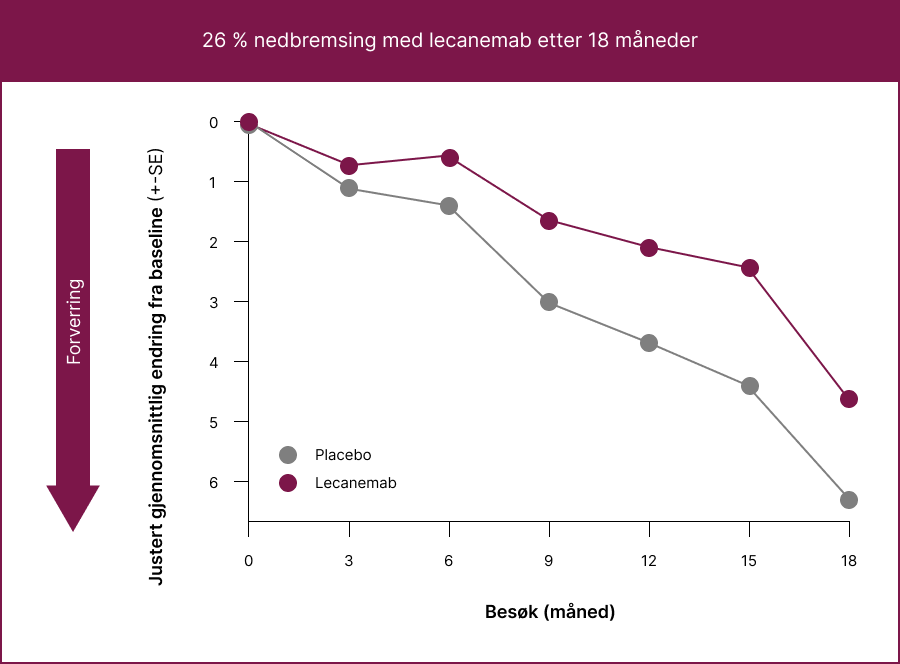
LEQEMBI bremset sykdomsprogresjonen betydelig i henhold til ADAS-Cog14-skalaen med 26 % etter 18 måneder og på alle tidspunkter fra 6 måneder.1
§ADAS-Cog14 = Alzheimer’s Disease Composite Score.
LEQEMBI fjerner effektivt amyloid-β plakk2
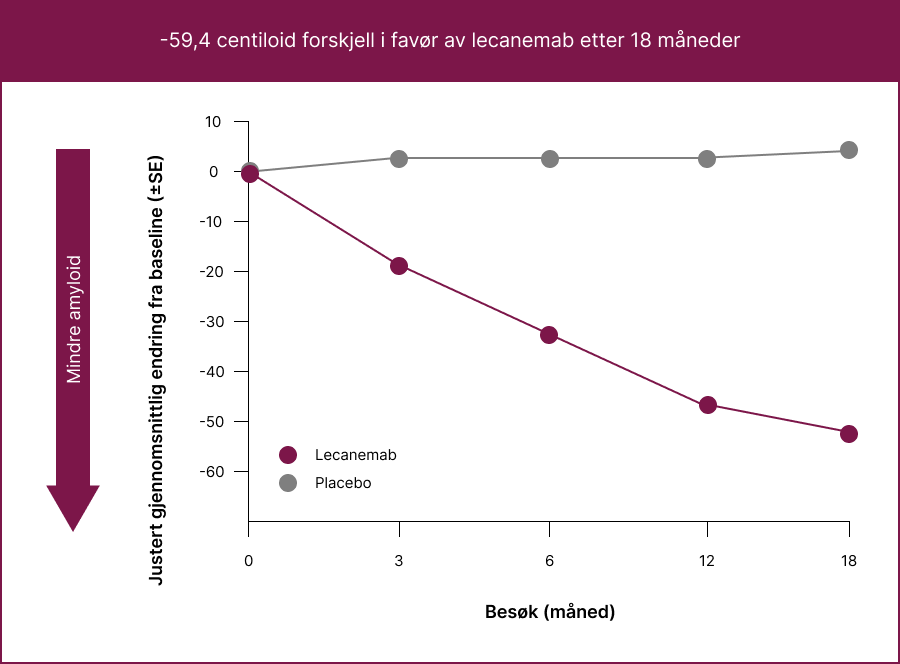
Effekten av LEQEMBI på nivåer av amyloid beta-plakk i hjernen ble evaluert ved hjelp av visuell PET-avbildning og kvantifisert ved hjelp av Standard Uptake Value Ratio (SUVR)-metoden og centiloidskalaen. Den gjennomsnittlige endringen fra baseline i forhold til placebo var statistisk signifikant for LEQEMBI 10 mg/kg annenhver uke i uke 79 i den indiserte populasjonen (-59,437).
Referanser
1. LEQEMBI Preparatomtale avsnitt 5.1
2. van Dyck CH, Swanson CJ, Aisen P, et al. Lecanemab in Early Alzheimer’s Disease. N Engl J Med. 2023;388(1):9−21.
3. Perry R. et al. Lecanemab for treatment of individuals with early Alzheimer’s Disease (AD) who are apolipoprotein E ε4 (ApoE ε4) non-carriers or heterozygotes. The Journal of Prevention of Alzheimer’s Disease. 2026:1-11(13)







