*31% mindre forverring av kognitive symptomer og funksjoner over 18 måneder hos lecanemab-behandlede pasienter sammenlignet med placebogruppen (gjennomsnittlig endring fra baseline ifølge CDR-SB var 1,22 sammenlignet med 1,75; forskjell mellom grupper −0,535; 95% KI −0,778; −0,293).1
LEQEMBI er den eneste godkjente anti-amyloid antistoffet med mindre enn 10% forekomst av ARIA- E 1
2% (16/757) av pasientene opplevde symptomatisk ARIA-E eller ARIA-H.
Ingen økt dødelighet i behandlingsgruppen sammenlignet med placebo (0,8% for LEQEMBI og 0,9% for placebo).
Behandlingsavbrudd på grunn av bivirkninger hos 7% i LEQEMBI-gruppen sammenlignet med 3% i placebogruppen.
De fleste radiologiske hendelser relatert til ARIA-E forekom tidlig i behandlingen (innen de første 7 dosene) og var stort sett milde (4%, n = 31/757) respektive moderate (4%, n = 33/757).
Risikoen for ARIA-relaterte radiologiske hendelser, inkludert symptomatiske og alvorlige, er forhøyet hos homozygote bærere av apolipoprotein E ε4 (ApoE ε4), sammenlignet med heterozygote bærere og ikke-bærere. LEQEMBI er derfor ikke indikert for bruk hos pasienter som er homozygote bærere av ApoE ɛ4.1

Sikkerheten for LEQEMBI har blitt evaluert hos 2 203 pasienter som har fått minst én dose av LEQEMBI. De vanligste bivirkningene hos den indikerte populasjonen var infusjonsrelaterte reaksjoner (26%), ARIA-H (13%), hodepine (11%) og ARIA-E (8,9%). Anfall, inkludert status epilepticus, har blitt rapportert ved behandling med LEQEMBI i kliniske studier.
De fleste infusjonsrelaterte reaksjonene skjedde ved den første infusjonen (75%, 178/237), og alvorlighetsgraden var stort sett mild (69%) eller moderat (28%).
ARIA kan oppstå spontant hos pasienter med Alzheimers sykdom. Behandling med LEQEMBI kan forårsake ARIA, enten i form av ARIA med ødem (ARIA-E) som kan observeres på MR som hjerneødem eller ødem i sulci, eller ARIA med hemosiderinutfelling (ARIA-H), som inkluderer mikroblødning og overfladisk siderose.
ARIA-H og ARIA-E kan forekomme sammen. Det var ingen økning av isolert ARIA-H (dvs. ARIA-H hos pasienter som ikke også fikk ARIA-E) for LEQEMBI sammenlignet med placebo.
Inkludert asymptomatiske radiologiske hendelser ble ARIA (ARIA-E og ARIA-H) observert hos 17% (128/757) av pasientene som fikk LEQEMBI sammenlignet med 7% (55/764) av pasientene som fikk placebo i studie 301 (indikerte populasjon).
Symptomatisk ARIA forekom hos 2% (16/757) av pasientene som fikk LEQEMBI, hvorav symptomer som krevde sykehusinnleggelse ble rapportert hos 0,4% (3/757).
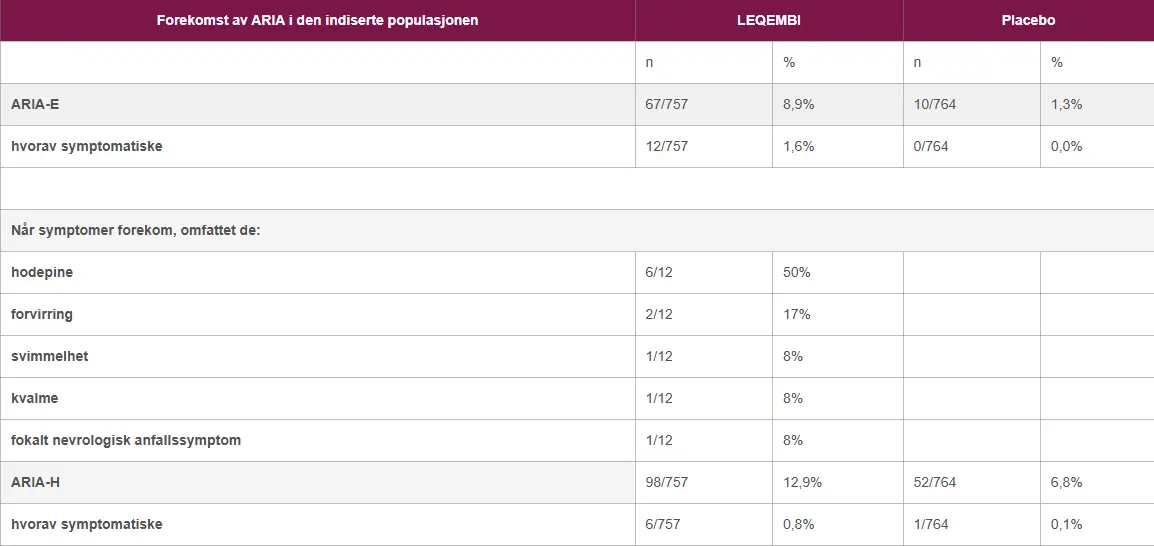
ARIA-E ble observert hos 9% (67/757) av pasientene som fikk LEQEMBI. Majoriteten av ARIA-E var asymptomatisk, mens symptomatisk ARIA-E ble rapportert hos 2% (12/757) av pasientene. Symptomer som ble rapportert i forbindelse med ARIA-E var hodepine (50%, 6/12), forvirring (17%, 2/12), svimmelhet (8%, 1/12) og kvalme (8%, 1/12). Fokale nevrologiske bortfall (8%, 1/12) forekom også.
Studie 301: CLARITY-AD, indikerte populasjon2
| Forekomst av ARIA i den indiserte populasjonen | LEQEMBI | Placebo | ||
|---|---|---|---|---|
| n | % | n | % | |
| ARIA-E | 67/757 | 8,9% | 10/764 | 1,3% |
| hvorav symptomatiske | 12/757 | 1,6% | 0/764 | 0,0% |
| . | ||||
| Når symptomer forekom, omfattet de: | ||||
| hodepine | 6/12 | 50% | ||
| forvirring | 2/12 | 17% | ||
| svimmelhet | 1/12 | 8% | ||
| kvalme | 1/12 | 8% | ||
| fokalt nevrologisk anfallssymptom | 1/12 | 8% | ||
| ARIA-H | 98/757 | 12,9% | 52/764 | 6,8% |
| hvorav symptomatiske | 6/757 | 0,8% | 1/764 | 0,1% |
- Intracerebrale blødninger større enn 1 cm i diameter ble rapportert hos 0,5% (4/757) av pasientene i studie 301 etter behandling med LEQEMBI, sammenlignet med 0,1% (1/764) av pasientene som fikk placebo. Tilfeller av hjerneblødning med dødelig utfall har blitt observert hos pasienter som har fått LEQEMBI. Det var ingen økt dødelighet i LEQEMBI-gruppen: 0,8% sammenlignet med 0,9% i placebogruppen.
Mer informasjon: Preparatomtale for LEQEMBI (lecanemab)
ARIA-H = Amyloid-relatert radiologisk avvikelse som involverer mikroblødning og hemosiderinutfelling.
ARIA-E = Amyloid-relatert radiologisk avvikelse som involverer hjerneødem
Referanser
1. LEQEMBI Preparatomtale Avsnitt 4.1, 4.4, 4.8
2. van Dyck CH, Swanson CJ, Aisen P, et al. Lecanemab in Early Alzheimer’s Disease. N Engl J Med. 2023;388(1):9−21.