Biomarkører i klinisk praksis
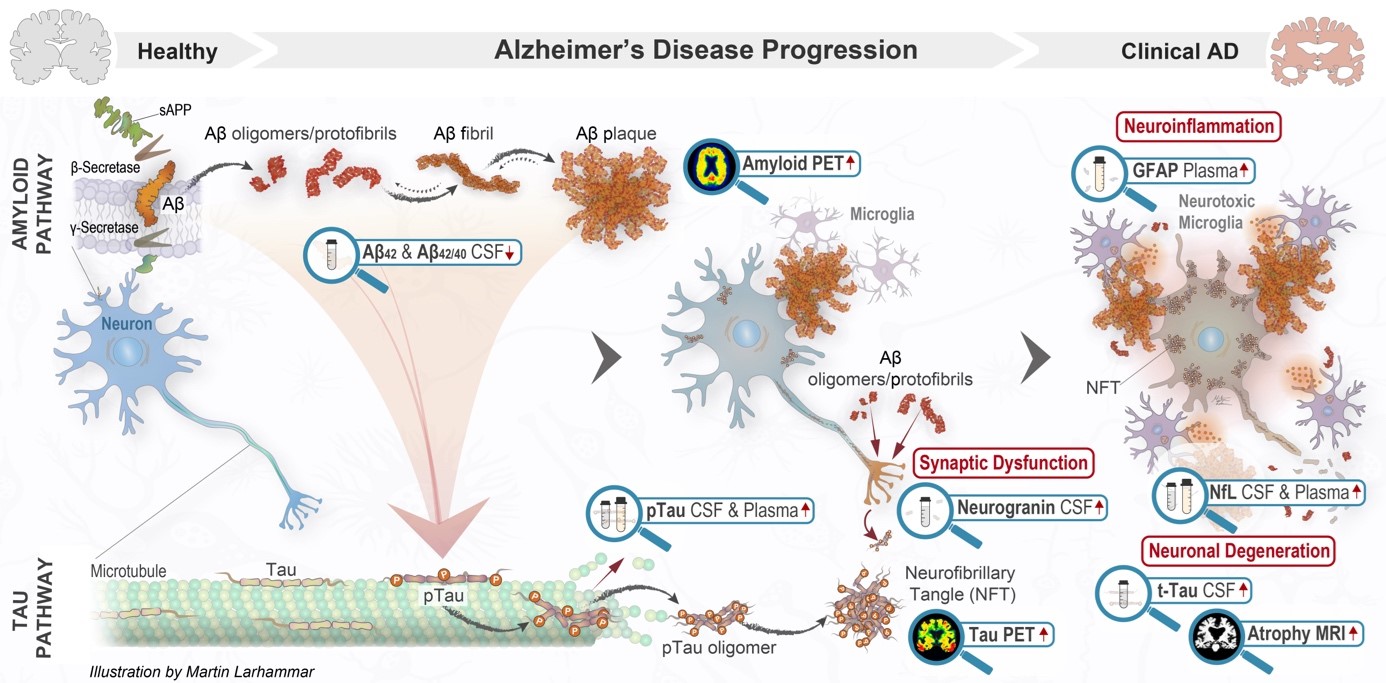
Fig 1 Referanser: 1. Jack et al. Revised criteria for diagnosis and staging of Alzheimer’s disease: Alzheimer’s Association Workgroup, Alzheimers Dement 2024 2. Hansson O, Biomarkers for neurodegenerative diseases, Nat Med. 2021
Biomarkører i cerebrospinalvæske
De mest tilgjengelige og brukte biomarkørene i Norden for Alzheimers sykdom (AD) er de som måles i cerebrospinalvæske. En vanlig såkalt ”AD-pakke” av prøver inkluderer Aβ42, Aβ40, fosforylert tau (P-tau) og total tau (T-tau). På grunn av den sterke korrelasjonen mellom P-tau og T-tau ved AD, er det sjelden relevant å tolke T-tau separat, bortsett fra i noen spesielle tilfeller, som ved mistenkt Creutzfeldt-Jacobs sykdom.1
Siden det finnes CSF-dynamiske variasjoner mellom pasienter, bør disse biomarkørene ikke tolkes individuelt, men helst som en ratio, for eksempel Aβ42/40 eller Aβ42/P-tau. Det er ikke uvanlig at alle markører er redusert eller økt uten noen underliggende patologisk prosess.1 En tilsynelatende normal Aβ42– eller P-tau-verdi, i kombinasjon med en klart avvikende ratio, bør derfor tolkes som forekomst av AD-patologi. Disse markørene regnes som såkalte Core 1-biomarkører (fig. 2) og kan primært brukes til å avgjøre om AD-endringer forekommer eller ikke. Core 2-biomarkører (fig. 2) er markører som kan gi et bilde av sykdommens patofysiologiske (biologiske) stadium. Disse biomarkørene er imidlertid fortsatt bare tilgjengelige innenfor rammen av forskningsstudier.1
Nevrofilament (NfL) måles ofte i kognitive vurderinger, men har begrenset verdi i utredningen av AD. NfL kan på gruppenivå vise hvor aktiv den nevrodegenerative prosessen er, men er normalt hos omtrent halvparten av alle pasienter med AD. Markøren er i stedet viktigere i differensialdiagnostikk ved mistanke om frontotemporallappsykdommer og atypisk Parkinsons sykdom, og er ofte forhøyet i tilfeller av vaskulær genese av kognitiv svikt.1-3
T-tau = Total-tau
P-tau = Fosforylert tau
NfL = Neurofilament
MCI = Mild kognitiv svikt
Non-p-tau = Ikke-fosforylert tau
Hvem skal testes med biomarkører?
Tolkning av testresultater basert på pretest-sannsynlighet
Ved høy pretest-sannsynlighet, for eksempel et typisk AD-syndrom hos en eldre person, kan man med stor sikkerhet stole på et positivt resultat (høy positiv prediktiv verdi). Et negativt resultat bør imidlertid tolkes med en viss forsiktighet, fordi det i denne sammenhengen har en lavere negativ prediktiv verdi. Det motsatte gjelder i tilfeller med lav pretest-sannsynlighet, for eksempel dersom pasienten kun har subjektive plager eller et klinisk syndrom som ikke er forenlig med AD.
Det stilles noen ganger spørsmål ved om eldre mennesker (over 80 år) bør testes med AD-biomarkører. Selv i denne aldersgruppen er biomarkørene generelt like pålitelige for å oppdage AD-patologi. Fordi det i denne alderen er vanlig å ha både ikke-symptomatisk AD-patologi og andre hjerneskader som kan forårsake kognitiv svikt, blir et positivt testresultat vanskeligere å tolke. En negativ test kan imidlertid brukes til å utelukke AD.5
Blodbaserte biomarkører for AD
I de senere årene har blodbaserte biomarkører utviklet seg raskt og viser nå lovende resultater i valideringsstudier.6,7 Den mest etablerte er plasma p-tau217, som har vist tilsvarende resultater sammenlignet med cerebrospinalvæske-markører. Dette har nå begynt å bli tilgjengelig i kliniske rutiner over hele verden, enten som en enkelt biomarkør eller som en ratio til Aβ42 eller ikke-fosforylert tau (non-p-tau). For tiden anbefales det kun til bruk på spesialiserte klinikker for kognitive lidelser, men i fremtiden vil det sannsynligvis være et viktig verktøy i utredningen allerede på primærhelsetjenestenivå.
| BIOMARKER CATEGORY | CSF or plasma analytes | Imaging |
|---|---|---|
| Core biomarkers | ||
| Core 1 | ||
| A (Aβ proteinopathy) | Aβ 42 | Amyloid PET |
| T1: (phosphorylated and secreted AD tau) | p-tau217, p-tau181, p-tau231 | |
| Core 2 | ||
| T2: (AD tau proteinopathy) |
MTBR-tau243, other phosphorylated tau forms (e.g., p-tau205), non-phosphorylated mid-region tau fragmentsa |
Tau PET |
| Biomarkers of non-specific processes involved in AD pathophysiology | ||
| N (injury, dysfunction, or degeneration of neuropil) | NfL | Anatomic MRI, FDG PET |
| I (inflammation) Astrocytic activation |
GFAP | |
| Biomarkers of non-AD copathology | ||
| V (vascular brain injury) | Infarction on MRI or CT, WMH | |
| S (α-synuclein) | αSyn-SAAa | |
Fig 2. Bearbeidet fra: Jack, C. R., Jr. et al. Revised criteria for diagnosis and staging of Alzheimer's disease: Alzheimer's Association Workgroup. Alzheimers Dement 20, 5143-5169 (2024).
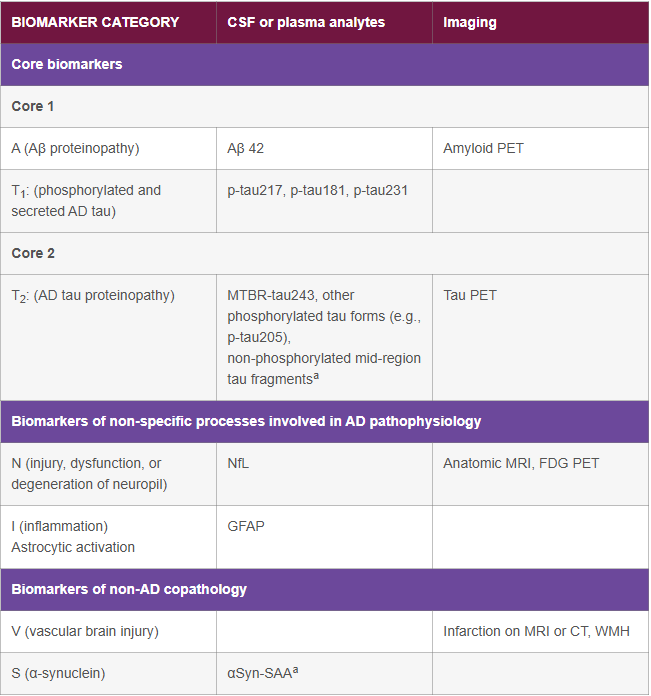
Fig 2.
Referanser
1. Jack CR, et al. Revised criteria for diagnosis and staging of Alzheimer’s disease: Alzheimer’s Association Workgroup. Alzheimers Dement. 2024;20(8):5143-69. doi:10.1002/alz.13859.
2. Olsson B, et al. CSF and blood biomarkers for the diagnosis of Alzheimer’s disease: a systematic review and meta-analysis. Lancet Neurol. 2016;15(7):673-84. doi:10.1016/S1474-4422(16)00070-3.
3. Ashton NJ, et al. A multicentre validation study of the diagnostic value of plasma neurofilament light. Nat Commun. 2021;12(1):3400. doi:10.1038/s41467-021-23620-z.
4. Shaw LM, et al. Appropriate use criteria for lumbar puncture and cerebrospinal fluid testing in the diagnosis of Alzheimer’s disease. Alzheimers Dement. 2018;14(11):1505-21. doi:10.1016/j.jalz.2018.07.220:
5. Jansen WJ, et al. Prevalence of cerebral amyloid pathology in persons without dementia: a meta-analysis. 2015;313(19):1924-38. doi:10.1001/jama.2015.4668.
6. Palmqvist S, et al. Blood biomarkers to detect Alzheimer disease in primary care and secondary care. 2024;332(15):1245-57. doi:10.1001/jama.2024.13855.
7. Palmqvist S, et al. Plasma phospho-tau217 for Alzheimer’s disease diagnosis in primary and secondary care using a fully automated platform. Nat Med. 2025;31(6):2036-43. doi:10.1038/s41591-025-03622-w.