Fra klinisk syndrom til biologisk definert diagnose med biomarkører
Fra klinisk syndrom til biologisk definert diagnose med biomarkører
Diagnostikk med og uten biomarkører
Å stille riktig diagnose av en kognitiv lidelse, som mild kognitiv svikt (eng. MCI), Alzheimers sykdom (eng. AD) eller annen nevrodegenerativ sykdom, er ofte utfordrende i fravær av biomarkører (f.eks. Aβ42/40 og p-tau).
Begrensninger med klinisk diagnose
En stor nevropatologisk studie har vist at en klinisk syndromdiagnose av Alzheimers sykdom ved spesialiserte klinikker for kognitiv sykdom var i samsvar med den nevropatologiske diagnosen i bare omtrent 70 % av tilfellene.1
En svensk studie viste lignende resultater der diagnostisk nøyaktighet etter undersøkelse ved en spesialisert hukommelsesklinikk (før tilgang til cerebrospinalvæskemarkører eller amyloid-PET) hadde en nøyaktighet på litt over 70 % sammenlignet med en biomarkørverifisert konsensusdiagnose.2 Studier som disse viser tydelig viktigheten av å inkludere biomarkører i evalueringen av pasienter ved en hukommelsesklinikk, spesielt ved mistanke om Alzheimers sykdom.
Nevropatologisk diagnose
Alzheimers sykdom var lenge en nevropatologisk diagnose, men i 1984 introduserte NINCDS-ADRDA Work Group kliniske kriterier for å diagnostisere ”sannsynlig” eller ”mulig” AD.3 Disse var basert på gradvis hukommelsessvekkelse (hukommelsesforstyrrelse), kognitiv svikt i minst ett ytterligere kognitivt domene, påvirkning på selvstendighet i hverdagsaktiviteter og utelukkelse av andre årsaker. Samsvaret med den nevropatologiske diagnosen var imidlertid lavt, og en endelig diagnose krevde fremdeles obduksjon.1
Biomarkørbasert diagnose: AA- og IWG-kriteriene
På slutten av 2010-tallet, med forbedrede biomarkører som amyloid-PET, tau-PET, blodbiomarkører og analyser av cerebrospinalvæske (CSF/spinalvæske), skjedde det et skifte mot en biologisk basert diagnostisk definisjon, i tråd med sykdommens patofysiologi.
To sentrale diagnostiske kriterier er kriteriene til Alzheimer’s Association (AA)4 og International Working Group (IWG)5. AA definerer Alzheimers sykdom basert på de underliggende patologiske endringene som kan oppdages med visse biomarkører (f.eks. amyloid PET, plasma p-tau217 eller cerebrospinalvæskeanalyse av Aβ42/40 eller Aβ42/p-tau), uavhengig av tilstedeværelsen av symptomer.6 Imidlertid fraråder disse kriteriene for øyeblikket diagnose i tilfeller av preklinisk sykdom (ingen objektivt verifiserbar kognitiv svikt). IWG krever både verifisering av patologi og objektivt verifiserbar kognitiv svikt for diagnose.7
I praksis prøver de fleste spesialiserte klinikker for kognitive lidelser i Norden å følge IWG-kriteriene, men i de fleste helseinstitusjoner er det mangel på tilgang til biomarkører, noe som betyr at ren klinisk syndromdiagnostikk fortsatt er vanlig til tross for usikkerheten. Slik diagnostikk fortsetter å tjene en funksjon når det gjelder pleie og behandling med symptomlindrende legemidler, men kan ikke brukes når man bruker legemidler som spesifikt retter seg mot de underliggende patologiene Aβ eller tau.
AT(N)-modellen og utvidede biomarkørkategorier
I det diagnostiske rammeverk til Alzheimer´s Association (AA) kartlegges tilstedeværelsen av amyloid-β (Aβ), tau og nevrodegenerasjon i henhold til den såkalte AT(N)-modellen. Der er N satt i parentes fordi det ikke er spesifikt for Alzheimers sykdom. I senere oppdateringer har rammeverket blitt utvidet til å omfatte inflammasjon (I), som er en viktig komponent ved AD og andre nevrodegenerative sykdommer, samt ko-patologiene vaskulær skade (V) og alfa-synuklein (S), som er årsaken til blant annet Lewy-legemer og Parkinsons sykdom.6
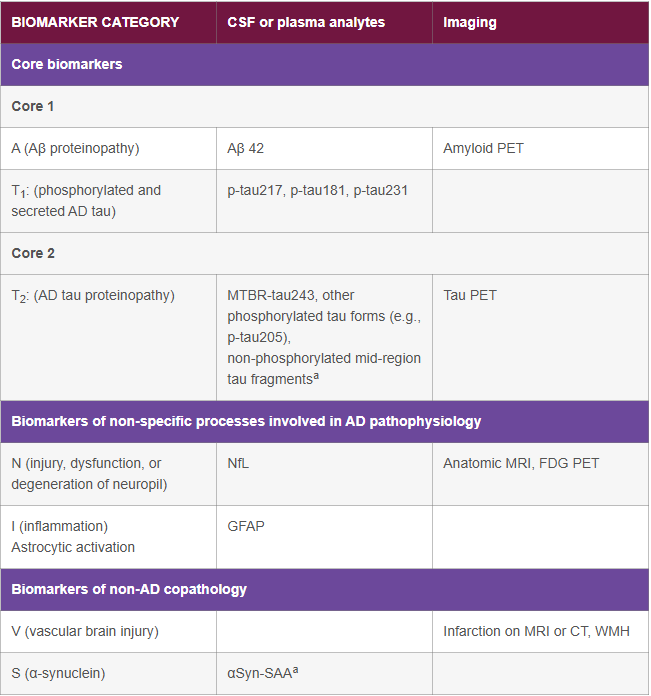
Det finnes mange forskjellige varianter av tau-patologi, og i en nylig oppdatering har den blitt delt inn i T1 (fosforylert og utskilt tau) og T2 (AD-tau-proteinopati). Se tabellen nedenfor for biomarkører for å måle kjernebiomarkører for A og T som definerer sykdommen, samt ikke-kjernebiomarkører for N, I, V og S.
| BIOMARKER CATEGORY | CSF or plasma analytes | Imaging |
|---|---|---|
| Core biomarkers | ||
| Core 1 | ||
| A (Aβ proteinopathy) | Aβ 42 | Amyloid PET |
| T1: (phosphorylated and secreted AD tau) | p-tau217, p-tau181, p-tau231 | |
| Core 2 | ||
| T2: (AD tau proteinopathy) |
MTBR-tau243, other phosphorylated tau forms (e.g., p-tau205), non-phosphorylated mid-region tau fragmentsa |
Tau PET |
| Biomarkers of non-specific processes involved in AD pathophysiology | ||
| N (injury, dysfunction, or degeneration of neuropil) | NfL | Anatomic MRI, FDG PET |
| I (inflammation) Astrocytic activation |
GFAP | |
| Biomarkers of non-AD copathology | ||
| V (vascular brain injury) | Infarction on MRI or CT, WMH | |
| S (α-synuclein) | αSyn-SAAa | |
Bearbeidet fra: Jack, C. R., Jr. et al. Revised criteria for diagnosis and staging of Alzheimer's disease: Alzheimer's Association Workgroup. Alzheimers Dement 20, 5143-5169 (2024).
Referanser
1. Beach TG, et al. Accuracy of the clinical diagnosis of Alzheimer disease at National Institute on Aging Alzheimer Disease Centers, 2005–2010. J Neuropathol Exp Neurol. 2012;71(4):266–73. doi:10.1097/NEN.0b013e31824b211b
2. Palmqvist S, et al. Blood biomarkers to detect Alzheimer disease in primary care and secondary care. JAMA. 2024;332(13):1245–57. doi:10.1001/jama.2024.13855
3. McKhann G, et al. Clinical diagnosis of Alzheimer’s disease: report of the NINCDS-ADRDA Work Group. Neurology. 1984;34(7):939–44. doi:10.1212/WNL.34.7.939
4. Jack CR Jr, et al. NIA-AA research framework: toward a biological definition of Alzheimer’s disease. Alzheimers Dement. 2018;14(4):535–62. doi:10.1016/j.jalz.2018.02.018
5. Dubois B, et al. Clinical diagnosis of Alzheimer’s disease: recommendations of the International Working Group. Lancet Neurol. 2021;20(6):484–96. doi:10.1016/S1474-4422(21)00066-1
6. Jack CR Jr, et al. Revised criteria for diagnosis and staging of Alzheimer’s disease: Alzheimer’s Association Workgroup. Alzheimers Dement. 2024;20(5):5143–69. doi:10.1002/alz.13859
7. Dubois B, et al. Alzheimer disease as a clinical-biological construct—an International Working Group recommendation. JAMA Neurol. 2024;81(5):487–98. doi:10.1001/jamaneurol.2024.3770