Patologien bak Alzheimers sykdom
Patologien ved Alzheimers sykdom begynner å utvikle seg flere tiår før de første symptomene dukker opp. Jo tidligere diagnosen stilles, desto større er sjansen for å bremse degenerasjonen og opprettholde hjernefunksjonen.1–5
Patologien ved Alzheimers sykdom begynner å utvikle seg mange år før sykdommen debuterer klinisk. Når symptomene på kognitiv svikt blir merkbare, har det allerede skjedd betydelig tap av synapser og celler.1–5 Derfor er det viktig å identifisere og diagnostisere pasienter med mild kognitiv svikt (MCI, Mild Cognitive Impairment) eller mild Alzheimers sykdom, da de kan ha nytte av tidlig intervensjon med et amyloid-β (Aβ) monoklonalt antistoff, for eksempel LEQEMBI®.
Alzheimers sykdom er en nådeløs nevrodegenerativ sykdom forårsaket av en kontinuerlig underliggende sykdomsprosess som begynner før og fortsetter etter avsetning av amyloid-β-plakk.1–5
Patologien ved Alzheimers sykdom antas å være initiert av dysmetabolisme av amyloid-β (Aβ)-peptider. Den ledende hypotesen om utviklingen av patologien ved Alzheimers sykdom slår fast at Alzheimers sykdom er forårsaket av dysmetabolisme av Aβ-peptider, noe som fører til en opphopning av Aβ i hjernen og utløser nedstrømseffekter, som tau-patologi, økt oksidativt stress og betennelse, synaptisk tap og neuronal degenerasjon.6,7
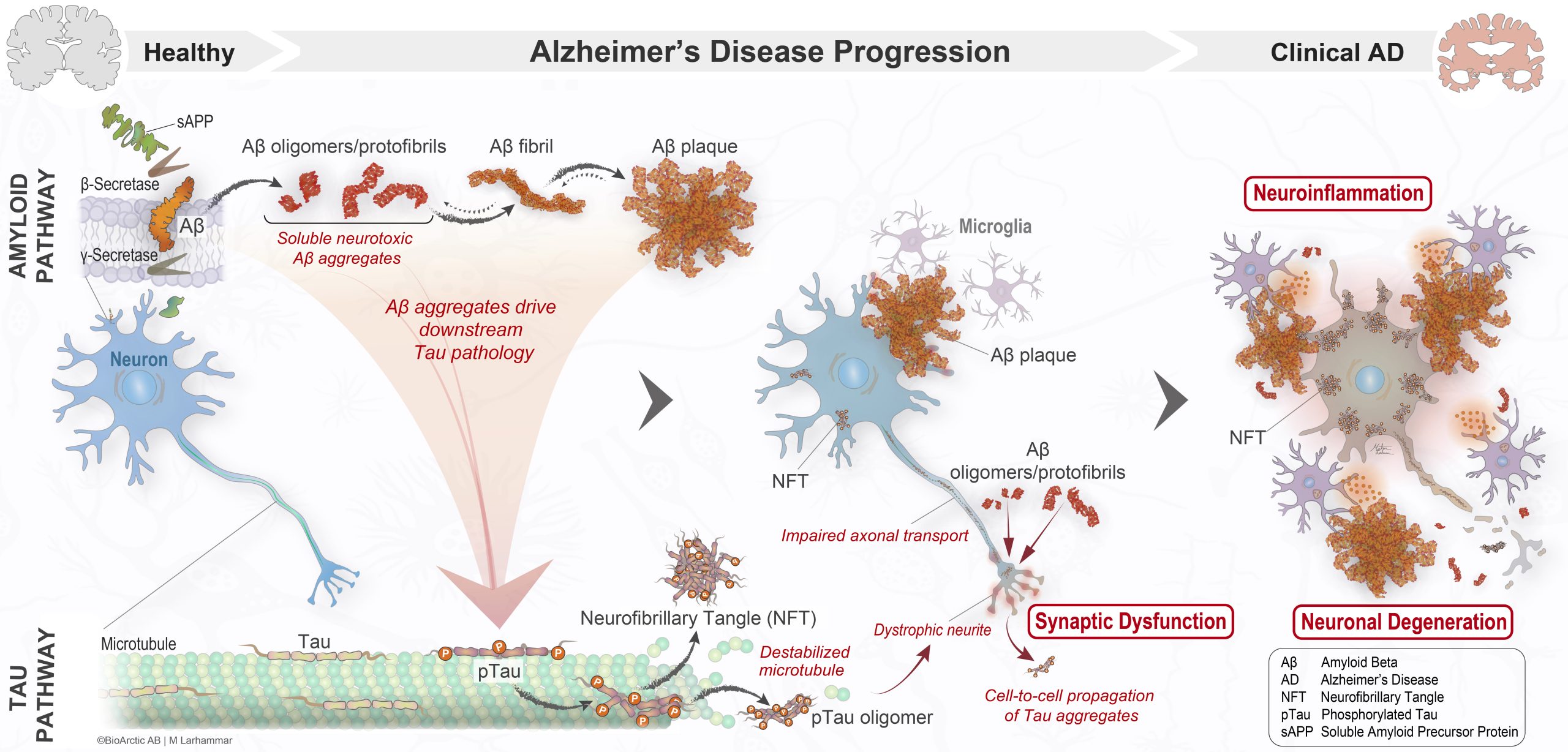
Figur 1. Patogenesen for Alzheimers sykdom.
Illustrasjonen viser en skjematisk oversikt over patologien ved Alzheimers sykdom fra en frisk tilstand til klinisk påvisbar Alzheimers, med fokus på to viktige, gjensidig avhengige patologiske veier, amyloidveien og tau-veien. Amyloidveien begynner med spalting av løselig amyloidprekursorprotein (sAPP) av β-sekretase og γ-sekretase, noe som fører til dannelsen av Aβ-peptid. Aβ danner løselige nevrotoksiske aggregater som utvikler seg fra små oligomerer til større løselige protofibriller, uløselige fibriller og til slutt Aβ-plakk (det patologiske kjennetegnet ved Alzheimers sykdom). Aβ-aggregater driver nedstrøms tau-patologi, inkludert hyperfosforylering av tau (pTau), noe som fører til destabilisering av mikrotubuli og svekket aksonal transport. Når pTau aggregerer, begynner det å akkumuleres intracellulært som nevrofibrillære tangler (NFT-er). Tau-aggregater antas å kunne spre seg fra ett område av hjernen til et annet, sannsynligvis fra celle til celle på en lignende måte som prioner. Aβ-oligomerer og protofibriller forstyrrer nevronfunksjonen, noe som fører til synaptisk dysfunksjon. En kritisk komponent i sykdomsprogresjonen er aktivering av mikroglia, noe som fører til svekket fysiologisk mikroglial funksjon og nevroinflammasjon. Aβ- og tau-patologi assosiert med uløst nevroinflammasjon forverrer til slutt synaptisk dysfunksjon og forårsaker synapsetap og nevrodegenerasjon som ligger til grunn for den kliniske presentasjonen av Alzheimers sykdom.
Referanser:
Serrano-Pozo A, et al. Plaque-associated local toxicity increases over the clinical course of Alzheimer disease. Am J Pathol. 2016 Feb;186(2):375–84. doi:10.1016/j.ajpath.2015.10.010 Paranjape GS, et al. Isolated amyloid-β(1–42) protofibrils, but not isolated fibrils, are robust stimulators of microglia. ACS Chem Neurosci. 2012 Apr 18;3(4):302–11. doi:10.1021/cn2001106 Jucker M, et al. Alzheimer’s disease: from immunotherapy to immunoprevention. Cell. 2023 Oct 12;186(21):4260–70. doi:10.1016/j.cell.2023.09.018 Tolar M, et al. The path forward in Alzheimer’s disease therapeutics: reevaluating the amyloid cascade hypothesis. Alzheimers Dement. 2020 Nov;16(11):1553–60. doi:10.1016/j.jalz.2019.09.075
Amyloidkaskadehypotesen
Amyloidkaskadehypotesen, opprinnelig foreslått av Hardy og Higgins (1992)6, innebærer at akkumulering av amyloid-β (Aβ)-peptider, spesielt Aβ42-isoformen, er den patologiske hendelsen som initierer Alzheimers sykdom. Dette har siden vært den sentrale hypotesen for patologien til Alzheimers sykdom og har dannet grunnlaget for utviklingen av både diagnostiske og terapeutiske metoder.
Ifølge den opprinnelige beskrivelsen utløser akkumulering av Aβ-peptid og avsetning i form av ekstracellulære amyloidplakk en kaskade av hendelser som omfatter følgende:1
Dannelse av nevrofibrillære tangler (NFT) fra hyperfosforylert tau-protein
Tap av integritet og økende dysfunksjon hos synapsene
Nevroinflammasjon
Nevrontap
Kognitiv lidelse
Alzheimers sykdom er kronisk og innebærer kontinuerlig akkumulering av løselige nevrotoksiske amyloid-β (Aβ)-former som svekker hjernefunksjonen. Aβ aggregeres og danner nevrotoksiske løselige Aβ-former (oligomerer og protofibriller) samt uløselig plakk. Aβ-peptidet har en sterk tendens til å aggregeres, og danne feilfoldede nevrotoksiske oligomerer og større løselige, dispergerbare strukturer kalt protofibriller. Etter hvert som de vokser, danner de Aβ-plakk, som er et av kjennetegnene på Alzheimers sykdom.1, 8-12
Aβ-tau-interaksjon: en mekanistisk kobling
Feillokalisert fosforylert tau løsner fra mikrotubuli, destabiliserer cytoskjelettet og svekker aksonal transport.14
Aβ-indusert tau-patologi som sprer seg transsynaptisk på en måte som ligner på prioner, sannsynligvis gjennom eksosommedierte eller reseptormedierte mekanismer.16
Eksperimentelle modeller viser at Aβ-reduksjon kan dempe tau-patologi, men tau-patologi alene er tilstrekkelig til å drive nevrodegenerasjon, noe som understreker den synergistiske toksisiteten til Aβ og tau.
Selv om de fleste dataene om tau-spredning fra celle til celle kommer fra in vitro– og in vivo-modeller, har de klare spatiotemporale mønstrene nylig blitt belyst in vivo hos mennesker ved hjelp av avbildningsteknikker som funksjonell magnetisk resonansavbildning (fMRI) og tau-PET.17
Rollen til betennelse og mikrogliaaktivering
Aβ-akkumulering aktiverer mikroglia og astrocytter og initierer en kronisk, uløst inflammatorisk respons som forverrer tau-patologien. Cytokiner som TNF-α, IL-1β og ROS kan i sin tur fremme tau-fosforylering og neuronalt stress ytterligere.18
Dette skaper en ond sirkel:
Den patologiske byrden ved Alzheimers sykdom utarmer clearing mekanismen til mikroglia.19
Alzheimers sykdom er en kronisk sykdom. Den økte amyloid-β-oppbyggingen er kontinuerlig gjennom hele sykdomsprogresjonen og fortsetter å utløse nedstrøms patologi, noe som forårsaker nedbrytning av synapser og nevronal degenerasjon. Hjernen til Alzheimers-pasienten er i en sårbar tilstand, og hver gjenværende synapse er viktig. Det som gjenstår må beskyttes.20
Aβ er nødvendig, men ikke utelukkende utløsende faktor for patologi.
Senere intervensjoner rettet mot Aβ kan vise seg å være mindre effektive på grunn av irreversibel tau-mediert skade og nevroinflammatorisk priming.
Kliniske studier med monoklonale antistoffer mot Aβ, inkludert LEQEMBI, støtter denne modellen.
LEQEMBI binder seg fortrinnsvis til løselige aggregater av Aβ14,15 og viser plakkfjerning og bremset forverring av kognitive symptomer når behandlingen igangsettes tidlig.
Referanser
1. Hampel H, et al. The amyloid-β pathway in Alzheimer’s disease. Mol Psychiatry. 2021 Oct;26(10):5481–5503. doi:10.1038/s41380-021-01249-0
2. Kumar A, et al. Alzheimer disease. In: StatPearls [Internett]. Treasure Island (FL): StatPearls Publishing; 2021 Aug 11 [sitert 2025 aug 20]. Tilgjengelig fra: https://www.ncbi.nlm.nih.gov/books/NBK499922/
3. Cummings J, et al. Alzheimer’s disease diagnostic criteria: practical applications. Alzheimers Res Ther. 2012 Sep 5;4(5):35. doi:10.1186/alzrt138
4. Jack CR, et al. NIA-AA Research Framework: toward a biological definition of Alzheimer’s disease. Alzheimers Dement. 2018 May;14(4):535–62. doi:10.1016/j.jalz.2018.02.018
5. Bateman RJ, et al. Clinical and biomarker changes in dominantly inherited Alzheimer’s disease. N Engl J Med. 2012 Aug 9;367(9):795–804. doi:10.1056/NEJMoa1202753
6. Hardy J, et al. Alzheimer’s disease: the amyloid cascade hypothesis. Science. 1992 Apr 10;256(5054):184–5. doi:10.1126/science.1566067
7. Selkoe DJ, et al. The amyloid hypothesis of Alzheimer’s disease at 25 years. EMBO Mol Med. 2016 Jun;8(6):595–608. doi:10.15252/emmm.201606210
8. Hong W, et al. Diffusible, highly bioactive oligomers represent a critical species in Alzheimer’s disease pathogenesis. Acta Neuropathol. 2018 Jul;136(1):19–40. doi:10.1007/s00401-018-1846-3
9. Shankar GM, et al. Amyloid-β protein dimers isolated from Alzheimer’s brains impair synaptic structure and function. Nat Med. 2008 Aug;14(8):837–42. doi:10.1038/nm1782
10. Walsh DM, et al. Naturally secreted oligomers of amyloid beta protein potently inhibit hippocampal long-term potentiation in vivo. Nature. 2002 Apr 4;416(6880):535–9. doi:10.1038/416535a
11. Hartley DM, et al. Protofibrillar intermediates of amyloid β-protein induce acute electrophysiological changes and progressive neurotoxicity in cortical neurons. J Neurosci. 1999 Oct 15;19(20):8876–84. doi:10.1523/JNEUROSCI.19-20-08876.1999
12. Sehlin D, et al. Large aggregates are the major soluble Aβ species in AD brain fractionated with density gradient ultracentrifugation. PLoS One. 2012 Feb 15;7(2):e32014. doi:10.1371/journal.pone.0032014
13. Pooler AM, et al. Propagation of tau pathology in Alzheimer’s disease: identification of novel therapeutic targets. Alzheimers Res Ther. 2013 May 29;5(4):49. doi:10.1186/alzrt203
14. Tapia-Rojas C, et al. It’s all about tau. Prog Neurobiol. 2019 Feb;15(2):226–40. doi:10.1016/j.jalz.2018.08.006
15. Guillozet AL, et al. Neurofibrillary Tangles, Amyloid, and Memory in Aginng and Mild Cognitive Impairment. Arch Neuro. 2003 Feb;105(2):148–53. doi:10.1007/s00401-002-0620-6
16. de Calignon A, et al. Propagation of tau pathology in a model of early Alzheimer’s disease. Neuron. 2012 Feb 23;73(4):685–97. doi:10.1016/j.neuron.2011.11.033
17. Lewis J, et al. Enhanced neurofibrillary degeneration in transgenic mice expressing mutant tau and APP. Science. 2001 Aug 24;293(5534):1487–91. doi:10.1126/science.1058189
18. Heneka MT, et al. Neuroinflammation in Alzheimer’s disease. Lancet Neurol. 2015 Apr;14(4):388–405. doi:10.1016/S1474-4422(15)70016-5
19. Streit WJ, et al. Dystrophic microglia in late-onset Alzheimer’s disease. Glia. 2020 Apr;68(4):845–54. doi:10.1002/glia.23782
20. McDade E, et al. Lecanemab in patients with early Alzheimer’s disease: detailed results of a randomized, double-blind, placebo-controlled, phase 3 trial. Alzheimers Res Ther. 2022;14:191. doi:10.1186/s13195-022-01033-9